對于初創(chuàng)企業(yè)而言,醫(yī)療器械產(chǎn)品從研發(fā)設計階段到走向消費市場,至少應經(jīng)歷醫(yī)療器械設計開發(fā)、醫(yī)療器械注冊檢測、醫(yī)療器械臨床試驗、醫(yī)療器械注冊申報、醫(yī)療器械生產(chǎn)許可申請等過程。
引言:對于初創(chuàng)企業(yè)而言,醫(yī)療器械產(chǎn)品從研發(fā)設計階段到走向消費市場,至少應經(jīng)歷醫(yī)療器械設計開發(fā)、醫(yī)療器械注冊檢測、醫(yī)療器械臨床試驗、醫(yī)療器械注冊申報、醫(yī)療器械生產(chǎn)許可申請等漫長的無盈利過程。那么,如何評估產(chǎn)品安全性風險、申報注冊周期、投入資金與成本?都是初創(chuàng)企業(yè)創(chuàng)始人最關(guān)心的問題。
基于上述問題,本文將按照產(chǎn)品設計開發(fā)、體系建立、創(chuàng)新產(chǎn)品申報(若涉及)、注冊檢測、臨床試驗、注冊申報、生產(chǎn)許可申請、產(chǎn)品上市等必要階段進行簡單介紹,希望對正踏步進軍醫(yī)療行業(yè)的初創(chuàng)企業(yè)有所幫助。
01 基本流程
(一)產(chǎn)品開發(fā)設計
1、產(chǎn)品設計開發(fā)流程
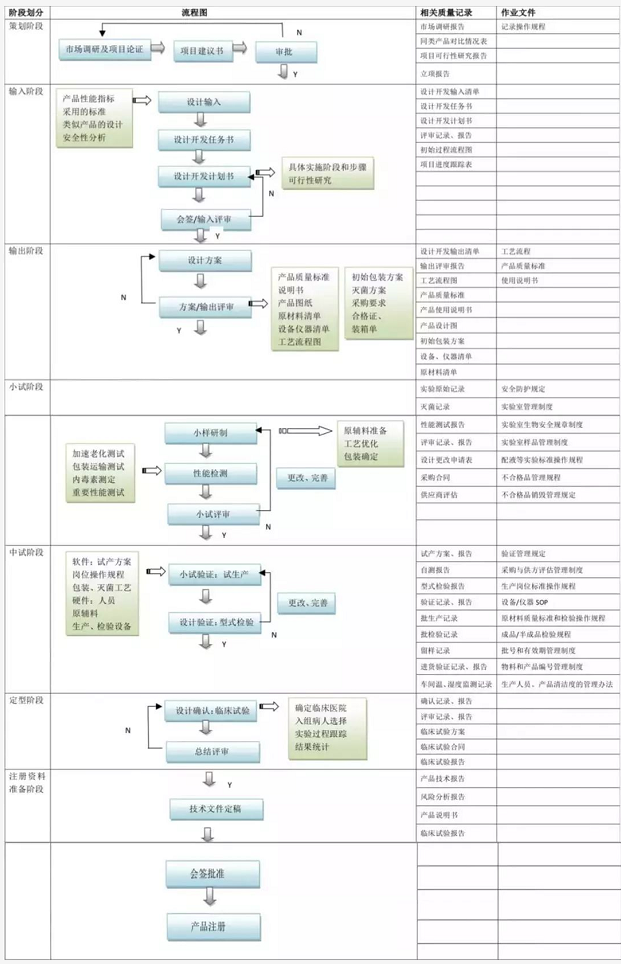
產(chǎn)品設計開發(fā)可分7個階段:策劃階段、設計輸入階段、設計輸出階段、小試階段、中試階段、定型階段、注冊資料準備階段。
2、產(chǎn)品設計開發(fā)要點
一般而言,創(chuàng)始人創(chuàng)立公司是基于科研成果與產(chǎn)品布局基礎上,并已初步具備研發(fā)團隊、合作伙伴等。但無論如何,對于初創(chuàng)公司而言,因涉及大量資金注入與技術(shù)攻堅,產(chǎn)品設計開發(fā)階段十分艱難,時間也是難以預估的,短則數(shù)月,長則數(shù)年。那么,如何在產(chǎn)品設計開發(fā)階段降低成本,滿足需求,增加創(chuàng)新?
首先,產(chǎn)品技術(shù)層面,專業(yè)高效的研發(fā)團隊是前提和基礎;其次,法規(guī)層面,建議尋找專業(yè)CRO公司或引進法規(guī)團隊對產(chǎn)品開發(fā)進行嚴格的風險評估,明確產(chǎn)品申報類型等。但我們常常發(fā)現(xiàn),很多新辦企業(yè)在產(chǎn)品已定型、開模后,才開始引進法規(guī)人員或?qū)ふ易稍儥C構(gòu)。此時的建議和措施往往基于補救,嚴重的可能涉及改模、重新設計等。所以對于新辦企業(yè)而言,法規(guī)前置慎重考量。最后,還應關(guān)注產(chǎn)品專利布局。公司應重點布局核心技術(shù)的知識產(chǎn)權(quán)保護,同時還應考慮核心技術(shù)轉(zhuǎn)讓、購買等問題,而產(chǎn)品的專利申報可以委托相應機構(gòu),后期若涉及專利較多,亦可引入兼職或?qū)B毴藛T。
3、創(chuàng)新醫(yī)療器械申報
2014年2月7日,CFDA發(fā)布了《創(chuàng)新醫(yī)療器械特別審批程序(試行)》(食藥監(jiān)械管〔2014〕13號),此文件自2014年3月1日起施行。該程序是在確保上市產(chǎn)品安全、有效的前提下,針對創(chuàng)新醫(yī)療器械設置的審批通道,但也有嚴苛的審批標準:(1)產(chǎn)品核心技術(shù)發(fā)明專利權(quán)。審批申請人經(jīng)過其技術(shù)創(chuàng)新活動,在中國依法擁有產(chǎn)品核心技術(shù)發(fā)明專利權(quán),或者依法通過受讓取得在中國發(fā)明專利權(quán)或其使用權(quán);或者核心技術(shù)發(fā)明專利的申請已由國務院專利行政部門公開。(2)國內(nèi)首創(chuàng)產(chǎn)品。主要工作原理/作用機理為國內(nèi)首創(chuàng),產(chǎn)品性能或者安全性與同類產(chǎn)品比較有根本性改進,技術(shù)上處于國際領(lǐng)先水平,并且具有顯著的臨床應用價值。(3)產(chǎn)品基本定型。申請人已完成產(chǎn)品的前期研究并具有基本定型產(chǎn)品,研究過程真實和受控,研究數(shù)據(jù)完整和可溯源。

若企業(yè)產(chǎn)品設計滿足上述要求,則應著手申報創(chuàng)新。創(chuàng)新特別審批是申請人已完成產(chǎn)品的前期動物研究并具有基本定型產(chǎn)品即可申報,申報流程詳見圖2。
據(jù)統(tǒng)計,截止目前,CMDE共計收到創(chuàng)新醫(yī)療器械特別審批申請近800項(其中,進口產(chǎn)品40余項),通過審查一共149項(進口13項)。審查通過率僅約20%。因此,對于初創(chuàng)企業(yè)來說,建議尋找專業(yè)的CRO團隊合作,提高申報成功率。
(二)體系建立
1、法規(guī)背景
為加強對醫(yī)療器械的監(jiān)督管理,提升企業(yè)質(zhì)量管理水平,保障醫(yī)療器械產(chǎn)品的安全有效,根據(jù)《醫(yī)療器械監(jiān)督管理條例》(國務院令650號)和《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》(國家食品藥品監(jiān)督管理總局令第7號),國家食品藥品監(jiān)督管理總局制定并印發(fā)了《關(guān)于發(fā)布醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范附錄無菌醫(yī)療器械的公告》(2015年第101號)、《關(guān)于發(fā)布醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范附錄植入性醫(yī)療器械的公告》(2015年第102號)及《關(guān)于發(fā)布醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范附錄體外診斷試劑的公告》(2015年第103號)。上述三個附錄是無菌醫(yī)療器械、植入性醫(yī)療器械及體外診斷試劑三類產(chǎn)品生產(chǎn)質(zhì)量管理規(guī)范的特殊要求,于2015年10月1日起正式施行。
與此同時,2017年9月1日,CFDA又發(fā)布《關(guān)于第一類、第二類醫(yī)療器械生產(chǎn)企業(yè)實施醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范有關(guān)工作的通知》(食藥監(jiān)辦械監(jiān)〔2017〕120號),文件強調(diào)自2018年1月1日起,所有醫(yī)療器械生產(chǎn)企業(yè)均應當符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》要求。
因此,醫(yī)療器械生產(chǎn)企業(yè)需嚴格按照法規(guī)要求建立質(zhì)量管理體系。而對于初創(chuàng)新公司除了體系建立,還需要面臨廠房選址和設計、建設等問題。
2、廠房規(guī)劃
對于廠房問題,需要根據(jù)產(chǎn)品管理類別進行考量。非無菌產(chǎn)品要求相對較低。若為無菌、體外診斷類產(chǎn)品,則應嚴格按照法規(guī)和標準選址,遠離有污染的空氣和水(如遠離鐵離、碼頭、機場、交通要道以及散發(fā)大量粉塵、屠宰場、染料等),對廠房的設計和裝修,必須請專業(yè)的團隊和公司來設計和施工,如行政區(qū)、生活區(qū)和輔助區(qū)不得相互防礙影響,空氣潔凈級別不同的潔凈室(區(qū))之間的靜壓差應大于5帕,潔凈室(區(qū))與室外大氣的靜壓差應大于10帕,空氣潔凈度級別進行合理布局,人流、物流走向應當合理,避免交叉污染,注意潔凈室的水池或地漏等。雖然委托專業(yè)公司負責,但整個過程,都需要專業(yè)體系人員進一步把關(guān),避免整改,比如消防、環(huán)評等通不過等。
3、人員配置
建立體系問題,初創(chuàng)團隊到底需要多少人?哪些崗位可以兼任?
必備崗位人員:生產(chǎn)負責人1名、研發(fā)部負責人1名、質(zhì)量負責人1名、專職檢驗員2名、總經(jīng)理1名;可兼任崗位人員:管理者代表1名,可由質(zhì)量負責人兼任;采購部負責人1名,可由研發(fā)老大兼任;銷售部負責人1名,可由產(chǎn)品經(jīng)理或總經(jīng)理兼任;行政部負責人1名,也可讓總經(jīng)理兼任;內(nèi)審員2名,持有內(nèi)審資格證的即可兼任,但2人不得在同部門;生產(chǎn)人員1名以上;
如此算來十多個崗位,兼任下來,至少應有6人以上,《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》及相關(guān)附錄中規(guī)定:“企業(yè)應當配備與生產(chǎn)產(chǎn)品相適應的專業(yè)技術(shù)人員、管理人員和操作人員,具有相應的質(zhì)量檢驗機構(gòu)或者專職檢驗人員的要求。要求生產(chǎn)負責人與質(zhì)量負責人不得兼任,專職檢驗員也不要兼任”,雖然明確了三個崗位不得兼任,但也明確提到,應配備相適應的人員,所以還是應當根據(jù)產(chǎn)品配備充足的人員,避免被開出不合格項目。
4、體系認知
對于初創(chuàng)團隊而言,我們應深知:首先,質(zhì)量管理體系是個系統(tǒng)工作,要有系統(tǒng)的觀念和思維。文件及記錄僅僅是整個系統(tǒng)的一部分,一個子系統(tǒng)而已,此外還有關(guān)鍵的管理控制子系統(tǒng),設計控制子系統(tǒng),生產(chǎn)制造子系統(tǒng)。需要與公司的培訓系統(tǒng),績效系統(tǒng),營銷系統(tǒng)等等結(jié)合互動。基于此,質(zhì)量管理體系對企業(yè)來說,是企業(yè)多年運行的標準化沉淀產(chǎn)物。其次,符合規(guī)范要求是醫(yī)療器械企業(yè)生存的底線。行業(yè)特殊性,即法規(guī)符合性。以往,只知道要符合法規(guī),但具體如何符合法規(guī)及指導觀念往往都是比較模糊的。當前法規(guī)的目標是確保質(zhì)量管理體系的有效性以持續(xù)生產(chǎn)安全有效的醫(yī)療器械產(chǎn)品。基于此,法規(guī)監(jiān)管并不希望企業(yè)三天兩頭修改技術(shù)文件,工藝文件等,而是應保障在當前法規(guī)要求下,可持續(xù)生產(chǎn)安全有效醫(yī)療器械產(chǎn)品。若日常工作中就對法規(guī)要求有所思慮,那么質(zhì)量管理體系法規(guī)符合性相對是較好的。再者,實施質(zhì)量管理體系的終極目的,不是為了一張認證證書,而是降低風險。對企業(yè)來說,若證書拿到就萬事大吉,那么企業(yè)發(fā)展必定不會長遠。監(jiān)管部門審核,監(jiān)督,你緊張;第三方審核你也緊張;大客戶來驗廠,估計十之八九你還是會緊張的。與其這樣,還不如老老實實的做好基礎,做好系統(tǒng)管理。更容易達到實施體系的目的:預防為主,降低風險。最后,我想說,沒有繼承,何來沉淀,何來文化。風來了,你是否準備好了?
(三)注冊檢驗
1、法規(guī)背景
《醫(yī)療器械分類界定管理辦法》明確規(guī)定,申請第二類、第三類醫(yī)療器械注冊,應當進行注冊檢驗。醫(yī)療器械檢驗機構(gòu)應當依據(jù)產(chǎn)品技術(shù)要求對相關(guān)產(chǎn)品進行注冊檢驗。注冊檢驗樣品的生產(chǎn)應當符合醫(yī)療器械質(zhì)量管理體系的相關(guān)要求,注冊檢驗合格的方可進行臨床試驗或者申請注冊。辦理第一類醫(yī)療器械備案的,備案人可以提交產(chǎn)品自檢報告。
2、注冊檢驗內(nèi)容
醫(yī)療器械注冊檢驗時檢驗機構(gòu)(必須是CFDA認可有資質(zhì)的機構(gòu))會依據(jù)企業(yè)所提供給的醫(yī)療器械產(chǎn)品技術(shù)要求做相應的檢驗,檢驗內(nèi)容主要包括安規(guī)性能檢驗,EMC電磁兼容性檢驗(有源產(chǎn)品需要,無源產(chǎn)品不需要),生物相容性檢驗等。
3、檢測周期
2017年3月15日,經(jīng)國務院批準,財政部發(fā)布《關(guān)于清理規(guī)范一批行政事業(yè)收費有關(guān)政策的通知》(財稅[2017]20號)。通知明確:自2017年4月1日起,包括醫(yī)療器械產(chǎn)品檢驗費在內(nèi)的多項事業(yè)性收費取消征收,這里包括醫(yī)療器械注冊檢驗收費。
據(jù)統(tǒng)計,CFDA認可的全國醫(yī)療器械檢驗機構(gòu)共有53家,各醫(yī)療檢驗機構(gòu)對這一政策事先并無充分預案,但又必須按時執(zhí)行。政策貌似助力行業(yè)發(fā)展,但短期內(nèi)卻給行業(yè)發(fā)展帶來諸多混亂。企業(yè)送檢就要排長隊,過去60個工作日即可完成的,現(xiàn)在200個工作日也未必能完成。有些機構(gòu)只接受本省樣品,跨省不接受,因為取消收費以后,經(jīng)費均由本省承擔,沒有充足的資源對外提供服務。當然,CFDA也逐漸意識到當下這種混亂局面,領(lǐng)導非常重視,并委派相關(guān)人員深入調(diào)研。
針對現(xiàn)狀,企業(yè)能做的就是在產(chǎn)品開發(fā)立項過程中引入專業(yè)法規(guī)人員把關(guān),協(xié)助研發(fā)工程師在設計之處就能明確遵循的標準和法規(guī)要求,降低后期整改難度。并在送檢前的開發(fā)階段做好充分的驗證測試,順利提高檢測通過率。
4、發(fā)展預測
不難發(fā)現(xiàn),中國的醫(yī)療器械注冊檢驗制度體系正在重構(gòu),并逐漸形成如下趨勢:首先,制造商應當注重構(gòu)建自己的自檢體系。因為放松管制意味著制造商將承擔更多的主體責任;其次,官方的檢驗機構(gòu)正在重新定位,明確自己新的職責,如繼續(xù)承擔監(jiān)督抽驗的任務,承擔強制性標準實施任務等等;最后,第三方檢驗機構(gòu)迎來新機遇。第三方檢驗機構(gòu)一直想在注冊檢驗領(lǐng)域為企業(yè)提供服務。過去沒有機會,現(xiàn)在機會出現(xiàn)了,大量第三方檢測機構(gòu)未來會有很多的機會參與到整個檢驗體系的構(gòu)建當中,分得一杯羹。檢驗資源增加了,企業(yè)會有更多的自主選擇權(quán),這是好事。未來檢驗體系的改革一定是有利于產(chǎn)業(yè)發(fā)展的。
(四)臨床評價
1、法規(guī)背景
《醫(yī)療器械注冊管理辦法》(國家食品藥品監(jiān)督管理總局令第4號)
《醫(yī)療器械臨床評價技術(shù)指導原則》(2015年第14號通告)
《醫(yī)療器械臨床試驗質(zhì)量管理規(guī)范》(國家食品藥品監(jiān)督管理總局/中華人民共和國國家衛(wèi)生和計劃生育委員會令第25號)
《關(guān)于醫(yī)療器械臨床試驗備案有關(guān)事宜的公告》(2015年第87號)
《免于進行臨床試驗的第二類醫(yī)療器械目錄》(2014年第12號通告)——488個II類產(chǎn)品
《免于進行臨床試驗的第三類醫(yī)療器械目錄》(2014年第13號通告)——79個III類產(chǎn)品
《第二批免于進行臨床試驗醫(yī)療器械目錄》(2016年第133號通告)——267個II類(含15個IVD),92個III類產(chǎn)品
《需進行臨床試驗審批的第三類醫(yī)療器械目錄》(2014年第14號的通告)——8個III類產(chǎn)品
《第三批免于進行臨床試驗醫(yī)療器械目錄》(2017年170號)——116個II類IVD,11個III類產(chǎn)品,37個II類產(chǎn)品
2、臨床評價路徑
臨床評價的三種途徑:對列入《免于進行臨床試驗的醫(yī)療器械目錄》中的產(chǎn)品,有條件的免于臨床試驗;對于同品種醫(yī)療器械臨床試驗或臨床使用獲得的數(shù)據(jù)進行分析評價;按照《醫(yī)療器械臨床試驗質(zhì)量管理規(guī)范》開展臨床試驗;
3、實施建議
產(chǎn)品若不在目錄內(nèi),則只能通過臨床試驗或臨床評價兩個途徑。對于新公司首款產(chǎn)品,條件允許的話,建議做臨床試驗。首先,免臨床途徑很難拿到經(jīng)驗數(shù)據(jù)和對比資料的授權(quán);其次,首款產(chǎn)品注冊上市后,其他產(chǎn)品注冊也會很快啟動,便于后續(xù)產(chǎn)品臨床工作開展。關(guān)于臨床試驗工作,對于初創(chuàng)團隊而言,建議委托第三方有實力、專業(yè)的CRO團隊,利于更快、更好的推進臨床進度。
(五)產(chǎn)品注冊申報
撰寫準備產(chǎn)品綜述資料、研究資料、生產(chǎn)制造信息 、臨床評價資料、產(chǎn)品風險分析資料、產(chǎn)品技術(shù)要求、產(chǎn)品注冊檢驗報告、說明書和標簽樣稿等資料清單,整理遞交CFDA。
(六)生產(chǎn)許可申請
1、法規(guī)背景
《醫(yī)療器械監(jiān)督管理辦法》明確規(guī)定:從事第二類、第三類醫(yī)療器械生產(chǎn)的,生產(chǎn)企業(yè)應當向所在地省、自治區(qū)、直轄市人民政府食品藥品監(jiān)督管理部門申請生產(chǎn)許可并提交其符合本條例規(guī)定條件的證明資料以及所生產(chǎn)醫(yī)療器械的注冊證。受理生產(chǎn)許可申請的食品藥品監(jiān)督管理部門應當自受理之日起30個工作日內(nèi)對申請資料進行審核,按照國務院食品藥品監(jiān)督管理部門制定的醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范的要求進行核查。對符合規(guī)定條件的,準予許可并發(fā)給醫(yī)療器械生產(chǎn)許可證;對不符合規(guī)定條件的,不予許可并書面說明理由。
根據(jù)現(xiàn)行法規(guī),醫(yī)療器械先注冊后許可。所以新辦企業(yè)會面臨一個特殊時期,拿到注冊證不能馬上銷售,需要申請“生產(chǎn)許可證”。以江蘇省為例,2014年12月22日,JSFDA發(fā)布《關(guān)于明確江蘇省第二類、第三類醫(yī)療器械生產(chǎn)企業(yè)注冊與生產(chǎn)許可環(huán)節(jié)質(zhì)量管理體系現(xiàn)場核查相關(guān)事宜的通知》(蘇食藥監(jiān)械管〔2014〕369號),通知明確:為減少重復現(xiàn)場考核、提高工作效率,第二類和第三類醫(yī)療器械首次注冊的現(xiàn)場考核與生產(chǎn)許可環(huán)節(jié)質(zhì)量管理體系現(xiàn)場考核,原則上合并進行。因此,對于新設企業(yè)首款產(chǎn)品而言,產(chǎn)品注冊證和生產(chǎn)許可證基本可以同步拿到。
2、申請周期
生產(chǎn)許可申請,法規(guī)規(guī)定為30個工作日,即1個月的時間。若現(xiàn)場審核無重大缺陷,并整改順利,基本上2-3個月即可拿到生產(chǎn)許可證。在此階段,公司可提前預熱,做好市場推廣,參展試用,但切記不可銷售。所以,在申請生產(chǎn)許可期間,公司基本上全部流程、文件都已形成,人員也已全部到位。萬事具備,只欠生產(chǎn)許可證。
3、生產(chǎn)許可證與注冊證差異
(1)醫(yī)療器械產(chǎn)品注冊證
醫(yī)療器械產(chǎn)品注冊證是醫(yī)療器械產(chǎn)品上市銷售的合格證明。第一類醫(yī)療器械產(chǎn)品備案,向市級食品藥品監(jiān)督管理局提交備案資料。第二類醫(yī)療器械產(chǎn)品注冊,向所在地省、自治區(qū)、直轄市食品藥品監(jiān)督管理部門提交注冊申請資料。第三類醫(yī)療器械產(chǎn)品注冊,注冊申請人應當向國家食品藥品監(jiān)督管理局(CFDA)提交注冊申請資料。
(2)醫(yī)療器械生產(chǎn)許可證
醫(yī)療器械生產(chǎn)許可證是醫(yī)療器械生產(chǎn)企業(yè)獲得醫(yī)療器械產(chǎn)品生產(chǎn)的資質(zhì)證明。從事第一類醫(yī)療器械生產(chǎn)的,向市食品藥品監(jiān)督管理局備案。從事第二類、第三類醫(yī)療器械生產(chǎn)的,省、自治區(qū)、直轄市食品藥品監(jiān)督管理局申請生產(chǎn)許可并提交相應的證明資料以及所生產(chǎn)醫(yī)療器械的注冊證。
02 費用預算與流程
產(chǎn)品注冊過程中,初創(chuàng)團隊最關(guān)心的就是費用及時間。以下為詳細流程表,涉及每個階段時限和費用。
(一)費用
對于資金投入,并未嚴格細化。但可粗算下:工商注冊費用可忽略不計;研發(fā)投入需結(jié)合具體產(chǎn)品和團隊,難以預估。但以5人的研發(fā)團隊計算,人力資源成本約100萬/年。廠房建立涉及廠房裝修和后期體系建設。廠房裝修和租賃費用,以1000平米計算,裝修約200萬人民幣。租金按照30元/平米/月計算,一年就是36萬,加上水電物業(yè)將近50萬。質(zhì)量體系建設是個系統(tǒng)工作,涉及產(chǎn)品的全生命周期,費用簡單預估50萬左右。注冊檢測不收費,若產(chǎn)品免臨床也不產(chǎn)生費用,做臨床的話根據(jù)產(chǎn)品而定,十幾萬至幾千萬都有可能。國產(chǎn)III類產(chǎn)品首次注冊費用為15.36萬,II類產(chǎn)品首次注冊費用則由各省級價格、財政部門制定。以江蘇省為例,II類產(chǎn)品首次注冊費用8.45萬元。小微企業(yè)提出的第二類醫(yī)療器械產(chǎn)品首次注冊申請,可免收首次注冊費。
(二)時間
時間方面,我們也可簡單粗算:廠房選址按照3個月計算,公司注冊耗時30個工作日左右;廠房裝修需3個月左右;若產(chǎn)品研發(fā)結(jié)束,已基本定型,可直接啟動注冊檢驗工作。無不合格項目修復或整改補檢,可按照150個工作日計算;若產(chǎn)品免臨床則相對簡單,做臨床的話則需根據(jù)產(chǎn)品而定,3個月至一兩年都是有可能的。資料準備充分后遞交CFDA受理,技術(shù)審評中心排隊審評并補正,預計耗時180個工作日。審評通過即可開展體系考核,若無重大缺陷項目,30個工作日后即可取得產(chǎn)品注冊證。II類和III類產(chǎn)品耗時差異主要體現(xiàn)在臨床方面,注冊檢驗和審評階段差異其實并不大。簡單算來,除去前期的準備階段,產(chǎn)品注冊耗時約:360工作日+臨床試驗時間。