- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
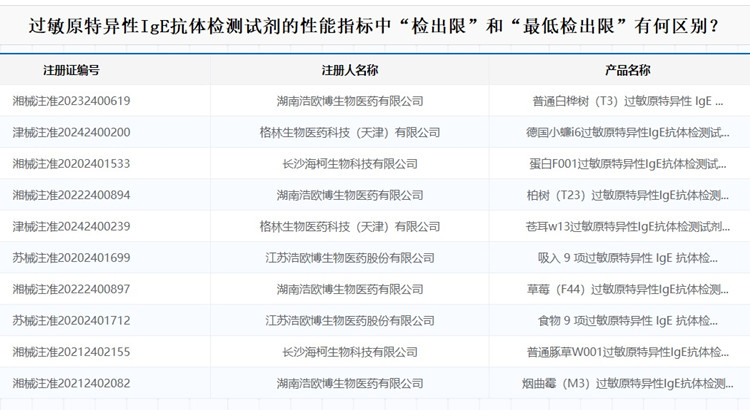
過敏原特異性IgE抗體檢測試劑的性能指標中“檢出限”和“最低檢出限”有何區別? 接著上一篇文章,繼續來給大家講解過敏原特異性IgE抗體檢測試劑注冊,說說這個常見的第二類體外診斷試劑注冊產品的特點,本文為大家介紹過敏原特異性IgE抗體檢測試劑的性能指標中“檢出限”和“最低檢出限”,一起看正文。 時間:2025-12-2 0:00:00 瀏覽量:30
-
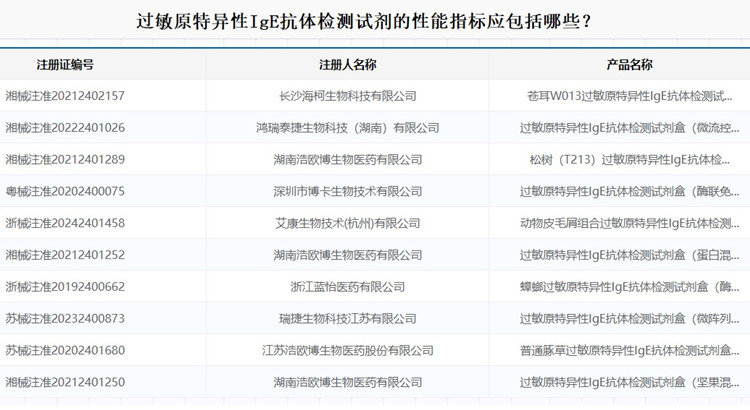
過敏原特異性IgE抗體檢測試劑的性能指標應包括哪些? 過敏原特異性IgE抗體檢測試劑是檢驗科最常見第二類體外診斷試劑注冊產品之一,本文為大家介紹過敏原特異性IgE抗體檢測試劑的性能指標應包括哪些?一起看正文。 時間:2025-12-2 0:00:00 瀏覽量:33
-
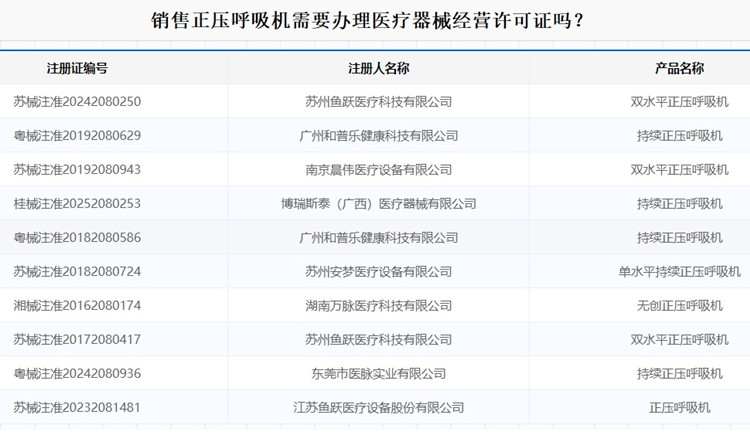
銷售正壓呼吸機需要辦理醫療器械經營許可證嗎? 正壓呼吸機適用于提供連續性呼吸道呼吸正壓,用于治療成人(體重大于30 kg)鼾癥、睡眠呼吸暫停低通氣綜合征。預期在家庭護理和專業醫療環境中使用,不用于生命支持。正壓呼吸機在家庭和醫療機構中廣泛使用,正好今天有客戶問到銷售正壓呼吸機是否需要辦理醫療器械經營許可證,因此,寫個文章說說這個事兒。 時間:2025-11-30 0:00:00 瀏覽量:71
-
正壓呼吸機注冊及醫療器械同品種比對臨床評價要點 正壓呼吸機由主機、濕化器、電源適配器(含電源線)、呼吸管路、面罩及應用附件、血氧模塊(選配)和數據傳輸模塊(選配)組成。適用于提供連續性呼吸道呼吸正壓,用于治療成人(體重大于30 kg)鼾癥、睡眠呼吸暫停低通氣綜合征。預期在家庭護理和專業醫療環境中使用,不用于生命支持。正壓呼吸機在我國屬于第二類醫療器械注冊產品,本文為大家介紹正壓呼吸機注冊及醫療器械同品種比對臨床評價要點 時間:2025-11-30 0:00:00 瀏覽量:61

-
進口轉國產醫療器械注冊體系常見問題之生產管理 對于進口轉國產醫療器械注冊質量管理體系來說,生產管理是體系核查的重點,當然,生產管理也是質量管理體系中最重要的模塊之一,本文為大家介紹生產管理常見問題,一起看正文。 時間:2025-11-29 0:00:00 瀏覽量:71

-
進口轉國產醫療器械注冊體系常見問題之采購模塊 對于進口轉國產醫療器械注冊體系核查來說,采購模塊也是問題高發區之一,采購是產品質量保證的重要模塊,也是產品功能、性能形成的基礎。本文為大家說說采購模塊常見問題,一起看正文。 時間:2025-11-29 0:00:00 瀏覽量:70

-
進口轉國產醫療器械注冊體系常見問題之質量控制 對于進口轉國產醫療器械注冊注冊事項來說,醫療器械質量管理體系建設及通過進口體系現場核查是關鍵愛你事項,本文為大家介紹有源醫療器械注冊產品的進口轉國產醫療器械注冊體系常見問題之質量控制,一起看正文。 時間:2025-11-28 0:00:00 瀏覽量:86

-
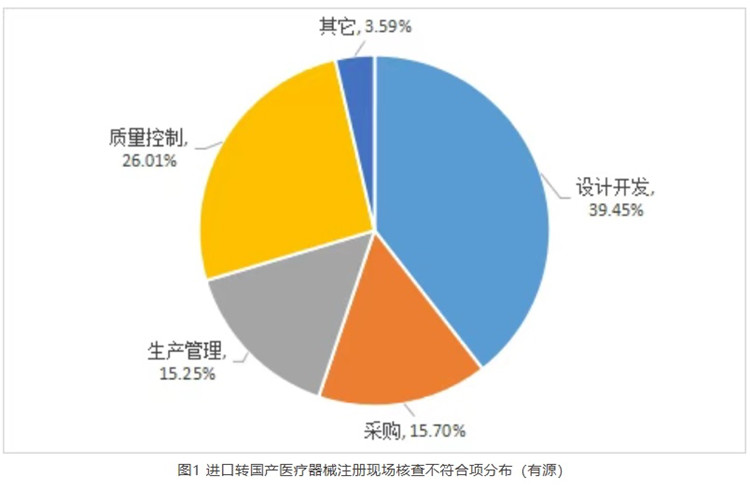
有源醫療器械進口轉國產醫療器械注冊體系常見問題之設計開發 隨著貫徹落實國辦《關于全面深化藥品醫療器械監管改革促進醫藥產業高質量發展的意見》的深入,我國醫療器械行業的快速發展及政策環境的持續優化,越來越多的跨國企業選擇將進口醫療器械轉移至中國境內生產。通過分析2025年上海市器審中心對進口轉國產的有源醫療器械開展注冊現場核查的情況,有源醫療器械進口轉國產注冊體系不符合項主要集中在設計開發、采購、生產管理與質量控制部分,合計占比96.41%。 時間:2025-11-28 0:00:00 瀏覽量:95
-
一次性支氣管成像導管注冊及醫療器械同品種比對臨床評價要點 一次性支氣管成像導管由主機插頭、連接線纜、操縱手柄、插入管、吸引管及注液閥組成。產品為經環氧乙烷滅菌的無菌產品。與電子內窺鏡圖像處理器、內窺鏡附件以及其他輔助設備配套使用以用于導氣管、氣管、支氣管樹內的內窺鏡檢查。一次性支氣管成像導管在我國屬于第二類醫療器械注冊產品,本文為大家介紹一次性支氣管成像導管注冊及醫療器械同品種比對臨床評價要點,一起看正文。 時間:2025-11-27 21:43:19 瀏覽量:102

-
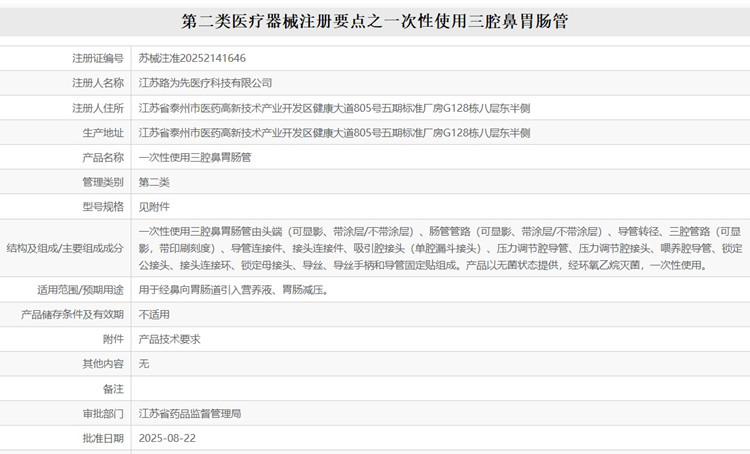
第二類醫療器械注冊要點之一次性使用三腔鼻胃腸管 一次性使用三腔鼻胃腸管由頭端、腸管管路、導管轉徑、三腔管路、導管連接件、接頭連接件、吸引腔接頭、壓力調節腔導管、壓力調節腔接頭、喂養腔導管、鎖定公接頭、接頭連接環、鎖定母接頭、導絲、導絲手柄和導管固定貼組成。產品以無菌狀態提供,經環氧乙烷滅菌,一次性使用。用于經鼻向胃腸道引入營養液、胃腸減壓。一次性使用三腔鼻胃腸管在我國屬于第二類醫療器械注冊產品,本文為大家介紹一次性使用三腔鼻胃腸管注冊要點。 時間:2025-11-27 0:00:00 瀏覽量:96
-
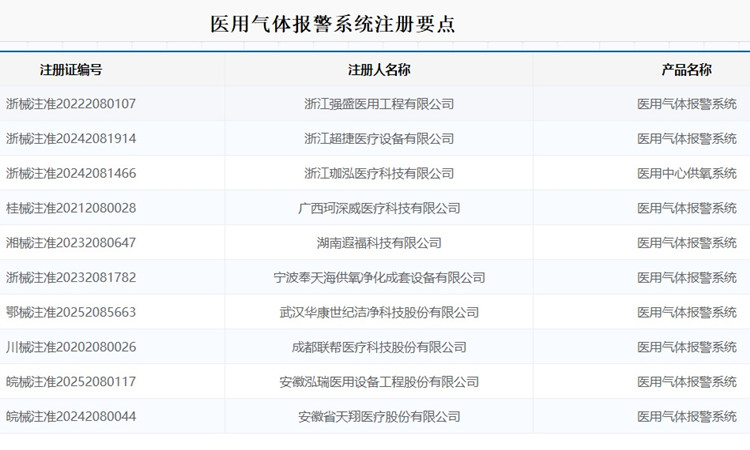
如何確定醫用氣體管道系統的報警功能是否應執行YY 9706.108? 醫用氣體報警系統通常由電源模塊、控制網絡模塊、顯示屏模塊、傳感器模塊、報警器面板和底盒組成。用于對醫院供氣系統的氧氣、醫療空氣、氮氣、二氧化碳、笑氣以及醫用真空進行壓力監測。醫用氣體報警系統在我國屬于第二類醫療器械注冊產品,本文為大家說說如何確定醫用氣體管道系統的報警功能是否應執行YY 9706.108?一起看正文。 時間:2025-11-26 0:00:00 瀏覽量:105
-
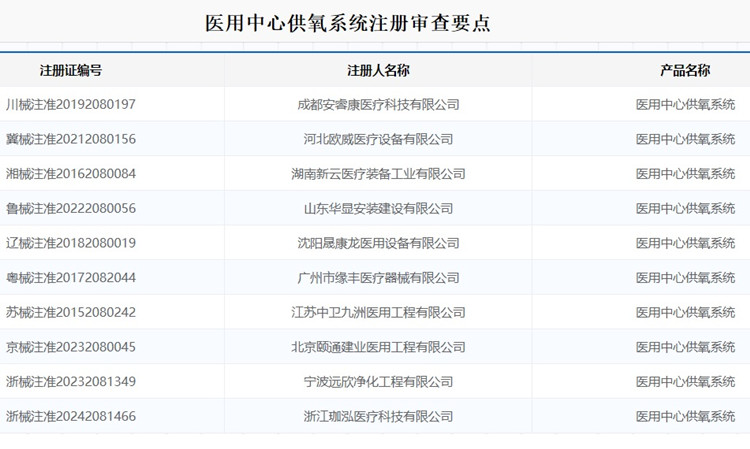
醫用中心供氧系統注冊審查要點 醫用中心供氧系統由中心供氧站(簡稱供氧站)、管道、二級減壓箱、閥門及終端送氧插頭、壓力監測報警裝置組成。其中,供氧站由高壓氧氣瓶(醫院自備)、匯流排、一級控制柜、管道及氧站報警裝置組成。產品將中心供氧站的氧氣通過減壓裝置和管道輸送到手術室、搶救室、治療室和各個病房的終端處,提供醫療使用。醫用中心供氧系統在我國屬于第二類醫療器械注冊產品,本文為大家說說醫用中心供氧系統產品注冊要點。 時間:2025-11-26 0:00:00 瀏覽量:140
-
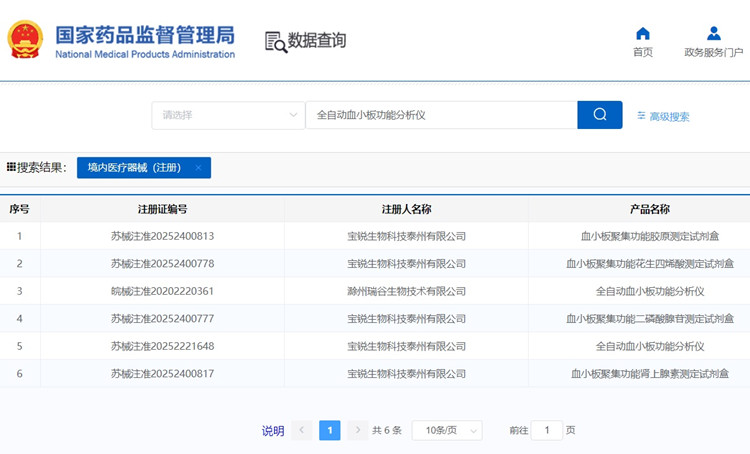
第二類醫療器械注冊要點之全自動血小板功能分析儀 全自動血小板功能分析儀由主機、配套軟件組成,其中主機由架體單元、樣本輸送單元、樣本搖勻單元、試劑倉單元、樣本穿刺單元、液路單元、以及電腦控制單元組成。軟件名稱:全自動血小板功能分析儀軟件。本產品與相應試劑配套使用,用于分析全血樣本中血小板數量、體積和聚集率相關參數。全自動血小板功能分析儀在我國屬于第二類醫療器械注冊產品,一起來看全自動血小板功能分析儀注冊要點。 時間:2025-11-25 0:00:00 瀏覽量:100
-
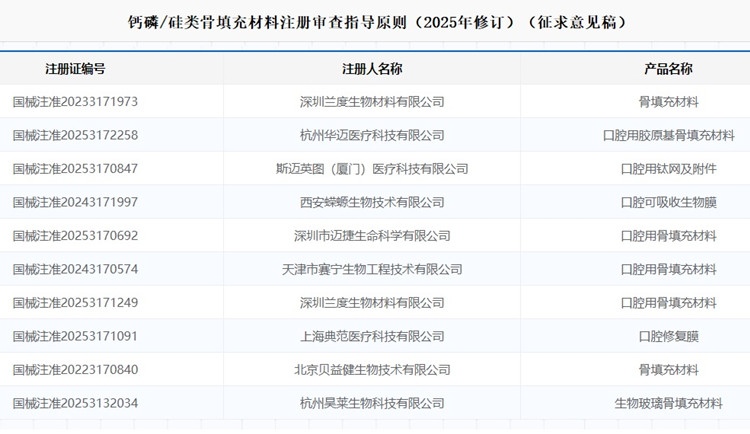
鈣磷/硅類骨填充材料注冊審查指導原則(2025年修訂)(征求意見稿) 2025年11月24日,國家藥監局發布《鈣磷/硅類骨填充材料注冊審查指導原則(2025年修訂)(征求意見稿)》,并面向公眾公開征求意見,一起來看具體內容。 時間:2025-11-25 0:00:00 瀏覽量:128
-
光固化氫氧化鈣蓋髓劑產品注冊審查指導原則(征求意見稿) 光固化氫氧化鈣蓋髓劑在我國屬于第三類醫療器械注冊產品,且在免于醫療器械臨床試驗目錄之內。2025年11月24日,國家藥監局發布《光固化氫氧化鈣蓋髓劑產品注冊審查指導原則(征求意見稿)》,本原則適用于蓋髓的光固化氫氧化鈣蓋髓劑,屬于通過外部能源使其固化的I類2型材料。一起來看具體內容。 時間:2025-11-24 0:00:00 瀏覽量:120

-
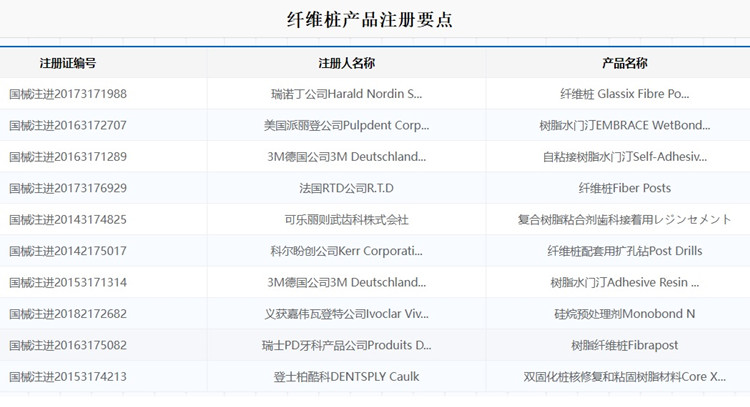
牙科纖維樁產品注冊審查指導原則(2025年修訂)(征求意見稿) 纖維樁在臨床上用于非活髓牙重建修復的固位材料,常見的名稱有樹脂纖維樁、纖維樁、玻璃纖維樁、個性化一體化纖維樁核、牙科纖維樁等,目前國產玻璃纖維樁注冊證還是較少,不少纖維樁還是進口醫療器械注冊產品。2025年11月24日,國家藥監局發布《牙科纖維樁產品注冊審查指導原則(2025年修訂)(征求意見稿)》,一起來看具體內容。 時間:2025-11-24 0:00:00 瀏覽量:129
-
個人未經許可在拼多多平臺銷售第三類醫療器械注冊產品被罰 部分電商平臺允許個人經營者,部分電商平臺需要個人工商戶或是公司這樣的法人實體作為經營者。對于個人經營者在電商平臺銷售醫療器械,同樣需要滿足醫療器械經營許可法規要求。近日,國家局通報典型醫療器械網絡銷售違規案例,其中許某未經許可在拼多多平臺銷售第三類醫療器械被罰案值得大家警醒,一起來看具體內容。 時間:2025-11-23 0:00:00 瀏覽量:177

-
攀枝花市某經營部在餓了么平臺銷售醫療器械,未按照規定告知監管部門被罰 網絡銷售越來越成為常見醫療器械流通渠道,同時也是醫療器械經營違規案件頻發領域,近日,國家藥監局公布典型的醫療器械網絡銷售違規案例,其中攀枝花市東區一心閣商貿經營部在餓了么平臺銷售醫療器械,未按照規定告知負責藥品監督管理的部門被罰,一起來看具體內容。 時間:2025-11-23 0:00:00 瀏覽量:133

-
對于免于進行臨床試驗的體外診斷試劑定量產品開展臨床試驗,最少需要多少例樣本? 對于免于進行臨床試驗的體外診斷試劑定量產品開展臨床評價時,入組樣本應符合什么要求?至少需要多少了臨床試驗樣本?一起看正文。 時間:2025-11-22 0:00:00 瀏覽量:149

-
體外診斷試劑產品編寫說明書【主要組成成分】項中“需要但未提供的試劑/軟件”應明確哪些內容? 體外診斷試劑產品編寫說明書【主要組成成分】項中“需要但未提供的試劑/軟件”應明確哪些內容? 時間:2025-11-22 0:00:00 瀏覽量:151

